Autor: XIA Qiuying, SUN Shuo, ZAN Feng, XU Jing, XIA Hui
Escola de Materiais Ciência e Engenharia, Universidade de Ciência e Tecnologia de Nanjing, Nanjing 210094, China
Resumo
Palavras-chaveï¼ LiSiON; filme fino eletrólito; bateria de lítio totalmente em estado sólido; bateria de filme fino
O rápido desenvolvimento da indústria de microeletrônica, como sistemas microeletromecânicos (MEMS), microssensores, cartões inteligentes e microdispositivos médicos implantáveis, leva a uma demanda crescente por dispositivos integrados armazenamento de energia de tamanho micro[1,2]. Entre as tecnologias de bateria disponíveis, bateria de lítio de película fina de estado sólido (TFLB) é considerada ideal fonte de energia para dispositivos microeletrônicos devido à sua alta segurança, tamanho pequeno, design power-on-chip, ciclo de vida longo e baixa taxa de autodescarga. Como um dos os principais componentes do TFLB, o eletrólito de filme fino de estado sólido desempenha um papel vital papel na determinação das propriedades do TFLB[3]. Portanto, desenvolver eletrólito de filme fino de estado sólido de alto desempenho é sempre uma tarefa objetivo importante para o desenvolvimento da TFLB. Atualmente, o mais utilizado o eletrólito no TFLB é o oxinitreto de fósforo e lítio amorfo (LiPON), que tem condutividade iônica moderada (2×10-6 Sâcm-1), baixa condutividade eletrônica (~10-14 Sâcm-1), ampla tensão janela (~5,5 V) e boa estabilidade de contato com lítio[4,5]. No entanto, a sua a condutividade iônica é relativamente baixa, o que impede o desenvolvimento futuro de TFLB de alta potência para a próxima era da Internet das Coisas (IoT)[6]. Assim, é urgente desenvolver novos eletrólitos de película fina com maior condutividade iônica, bem como grande janela de tensão e boa estabilidade de contato com lítio para TFLB de próxima geração.
Entre vários materiais eletrolíticos inorgânicos de estado sólido, o sólido Li2O-SiO2 sistema de solução e suas fases deuterogênicas foram identificadas como potenciais eletrólitos de filme devido à sua rápida condução tridimensional de lítio canais[7]. Por exemplo, Chen, et al.[8] relatado que o eletrólito sólido Li4.4Al0.4Si0.6O4-0.3Li2O substituído por Al tem uma alta condutividade iônica de 5,4×10-3 Sâcm-1 a 200 â. Adnan, et al.[9] descobriram que o composto Li4Sn0.02Si0.98O4 possui um valor máximo de condutividade de 3,07×10-5 Sâcm-1 à temperatura ambiente. No entanto, trabalhos anteriores em sistemas eletrolíticos Li2O-SiO2 focados principalmente em pó materiais com alta cristalinidade, enquanto trabalhos muito limitados foram relatados sobre suas contrapartes de filme fino amorfo para TFLB. Como o TFLB é normalmente construído depositando filmes finos de cátodo, eletrólito e camada anódica por camada, o filme eletrolítico deve ser preparado em temperatura relativamente baixa para evitar as interações desfavoráveis entre o cátodo e o eletrólito, o que resulta em rachadura e curto-circuito do TFLB[1,2]. Por isso, desenvolvendo eletrólito Li2O-SiO2 com característica amorfa preparado em baixo a temperatura é importante para TFLB. Embora trabalhos recentes[6] mostrem que uma alta condutividade iônica de lítio de 2,06 × 10-5 Sâcm-1 pode ser obtida por Li-Si-P-O-N amorfo filme fino, sua estabilidade de contato com os eletrodos e eletroquímica a estabilidade no TFLB ainda não foi investigada. Portanto, é criticamente importante desenvolver eletrólito de filme fino baseado em Li2O-SiO2 de alto desempenho e demonstrar sua aplicação real no TFLB.
Neste trabalho, o filme fino de oxinitreto de silício e lítio amorfo (LiSiON) foi preparado por pulverização catódica de magnetron de radiofrequência (RF) à temperatura ambiente e investigado como eletrólito de estado sólido para TFLB. O poder de pulverização catódica e o fluxo de gás de trabalho N2/Ar foi otimizado para obter a melhor condição de deposição para o filme fino LiSiON. Além disso, para demonstrar a aplicabilidade do eletrólito LiSiON otimizado para TFLB, uma célula completa MoO3/LiSiON/Li foi construída e seu o desempenho eletroquímico foi sistematicamente investigado.
1 Experimental
1.1 Preparação de filmes finos de LiSiON
Filmes finos de LiSiON foram preparados por pulverização catódica com magnetron RF (Kurt J. Lesker) usando um alvo de Li2SiO3 (76,2 mm de diâmetro) em temperatura ambiente por 12h. Antes da deposição, a pressão da câmara foi reduzida para menos de 1 x 10-5 Pa. A distância do alvo ao substrato foi de 10 cm. As amostras depositados sob potência de RF de 80, 100 e 120 W no fluxo de 90 sccm N2 são marcado como amostra LiSiON-80N9, LiSiON-100N9 e LiSiON-120N9, respectivamente. E as amostras depositadas sob potência de RF de 100 W no fluxo de 90 sccm N2 e 10 sccm Ar, 90 sccm N2 e 50 sccm Ar, 50 sccm N2 e 50 sccm Ar são marcados como amostra LiSiON-100N9A1, LiSiON-100N9A5 e LiSiON-100N5A5, respectivamente.
O filme MoO3 foi preparado por magnetron reativo de corrente contínua (DC) pulverização catódica (Kurt J. Lesker) usando um alvo de metal puro Mo (76,2 mm de diâmetro) de acordo com nosso relatório anterior[10]. A distância do alvo ao substrato foi de 10 cm, e DC a potência de pulverização catódica foi de 60 W. A deposição foi realizada no substrato temperatura de 100 â por 4 h na vazão de 40 sccm Ar e 10 sccm O2, seguido por um tratamento de recozimento in-situ a 450°C por 1 h. LiSiON-100N9A1 foi então depositado no filme MoO3 como eletrólito. Depois disso, um filme metálico de lítio com cerca de 2 Î1⁄4m de espessura foi depositado no filme LiSiON por evaporação térmica a vácuo (Kurt J. Lesker). A etapa final de fabricação envolveu a deposição do coletor de corrente de Cu e o processo de encapsulamento.
As estruturas cristalinas de as amostras foram caracterizadas por difração de raios X (XRD, Bruker D8 Advance). As morfologias e microestruturas das amostras foram caracterizadas por campo microscópio eletrônico de varredura de emissão (FESEM, FEI Quanta 250F) equipado com espectroscopia de raios X de energia dispersiva (EDS). As composições elementares do as amostras foram analisadas por espectrometria de massa com plasma indutivamente acoplado (ICP-MS, Agilent 7700X). A composição química e informações de ligação das amostras foram medidos por espectroscopia de fotoelétrons de raios X (XPS, Escalab 250XI, Thermo Científico).
1.4 Medições eletroquímicas
A condutividade iônica do eletrólito de filme fino LiSiON foi medida usando uma estrutura sanduíche de Pt/LiSiON/Pt. A impedância eletroquímica espectroscopia (EIS) (de 1000 kHz a 0,1 Hz com amplitude potencial de 5 mV) e medições de voltametria cíclica (CV) das amostras foram realizadas no Estação de trabalho eletroquímica biológica VMP3. Carga/descarga galvanostática (GCD) a medição do MoO3/LiSiON/Li TFLB foi realizada usando um Neware BTS4000 sistema de bateria em um porta-luvas cheio de argônio à temperatura ambiente. Um Sartório Balança Analítica (CPA225D, com resolução de 10 Î1⁄4g) foi utilizada para determinar a carga de massa do eletrodo e a carga de massa do filme de MoO3 são cerca de 0,4 mgâcm-2.
2 Resultados e discussão
Conforme mostrado na imagem óptica inserida na Fig. 1(a), um O alvo Li2SiO3 foi empregado para preparar filme fino de LiSiON. O resultado XRD na Fig. 1(a) revela que o alvo é composto pelo principal Li2SiO3 (JCPDS 83-1517) e fase secundária de SiO2. A medição ICP-MS indica que o átomo a proporção de Li: Si é de cerca de 1,79: 1 no alvo. Transparente amorfo fino filme foi obtido para a amostra típica LiSiON-100N9A1 após pulverização catódica do alvo (Fig. 1 (b)). A espessura da amostra típica LiSiON-100N9A1 medida a partir do A imagem FESEM de seção transversal na Fig. 1(c) é cerca de 1,2 Î1⁄4m, indicando uma taxa de crescimento de cerca de 100 nmâh-1 sob esta condição. Conforme mostrado na imagem FESEM de vista superior na Fig. 1(d), o a superfície do filme fino LiSiON é muito lisa e densa, sem rachaduras ou furos, tornando-o um eletrólito sólido adequado para TFLB para evitar atalhos e problema de segurança.
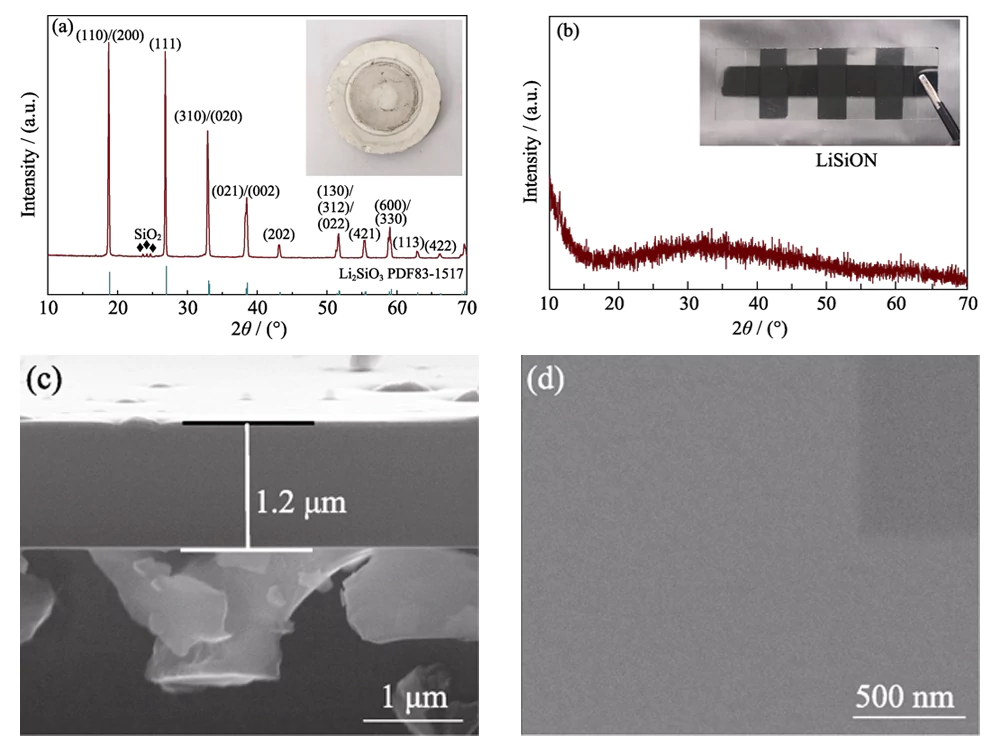
Figura 1 (a) padrão de XRD e imagem óptica do alvo de Li2SiO3; (b) Padrão XRD e imagem óptica de amostra típica LiSiON-100N9A1; (c) Seção transversal e (d) imagens FESEM de vista superior da amostra típica LiSiON-100N9A1
A análise XPS foi realizada para investigar a composição química e informações de ligação do alvo Li2SiO3 e da amostra típica LiSiON-100N9A1. A pesquisa XPS espectros de varredura na Fig. 2(a) revelam a presença de elementos Li, Si e O no alvo Li2SiO3 e a introdução do elemento N no filme fino LiSiON. A razão atômica de N: Si no filme fino LiSiON é cerca de 0,33: 1 de acordo com o resultado XPS. Combinando com a razão atômica correspondente (1,51: 1) obtida pelo ICP-MS medição, a estequiometria da amostra típica LiSiON-100N9A1 é determinado como sendo Li1.51SiO2.26N0.33. Comparado com o pico único de Si-Si (103,2 eV) no Espectro XPS de nível central Si2p do alvo Li2SiO3 (Fig. 2(b)), pico adicional de Si-N (101,6 eV) pode ser observado no filme fino LiSiON, sugerindo a ocorrência de nitretação em LiSiON[11,12]. Os O1 espectro XPS de nível central do alvo Li2SiO3 na Fig. 2(c) mostra dois ambientes de ligação: 531,5 eV originados de SiOx e 528,8 eV atribuído ao Li2O. Após a deposição, o componente adicional emergiu em 530,2 eV pode ser observado com filme fino LiSiON, que pode ser atribuído a não ponte oxigênio (On) em silicato[13,14]. O espectro XPS de nível central N1s de filme fino LiSiON na Fig. 2(d) pode ser deconvoluído em três picos, incluindo 398,2 eV para ligação Si-N, 396,4 eV para Li3N e 403,8 eV para espécies de nitrito NO2-, confirmando ainda mais a incorporação de N no Rede LiSiON[14,15,16]. Conforme ilustrado esquematicamente na Fig. 2(e), o a incorporação de N na rede LiSiON pode formar mais ligações cruzadas estrutura, o que é benéfico para a condução rápida de íons de lítio[6,17].
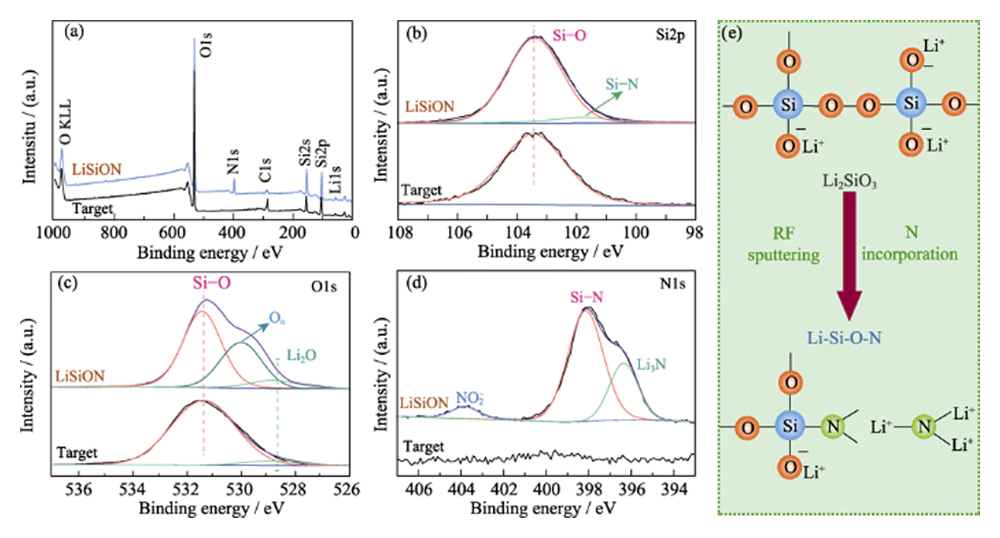
Fig. 2 (a) Varredura de pesquisa, (b) nível central Si2p, (c) nível principal O1s, e (d) espectros XPS de nível central N1s do alvo Li2SiO3 e amostra típica LiSiON-100N9A1; (e) Ilustração esquemática da mudança parcial da estrutura de Li2SiO3 para LiSiON com a incorporação de N
Para otimizar a condutividade iônica e a estabilidade eletroquímica do Filmes finos de LiSiON, vários filmes finos de LiSiON depositados em diferentes pulverizações potências e fluxos de gás de trabalho foram comparados em termos de sua iônica condutividades e janelas de tensão. Os gráficos de Nyquist à temperatura ambiente do Filmes finos de LiSiON são representados na Fig. 3(a) e a estrutura sanduíche Pt/LiSiON/Pt correspondente e o circuito equivalente são mostrado na Fig. 3(b). Como observado, os gráficos de Nyquist exibem um único semicírculo e dielétrico cauda de capacitância, que é característica do dielétrico condutor de filme fino com processo de relaxamento em massa imprensado entre contatos de bloqueio [17]. O iônico condutividades (Ïi) dos filmes finos de LiSiON podem ser calculadas usando a Eq. (1).
Ïi=d/(RA)
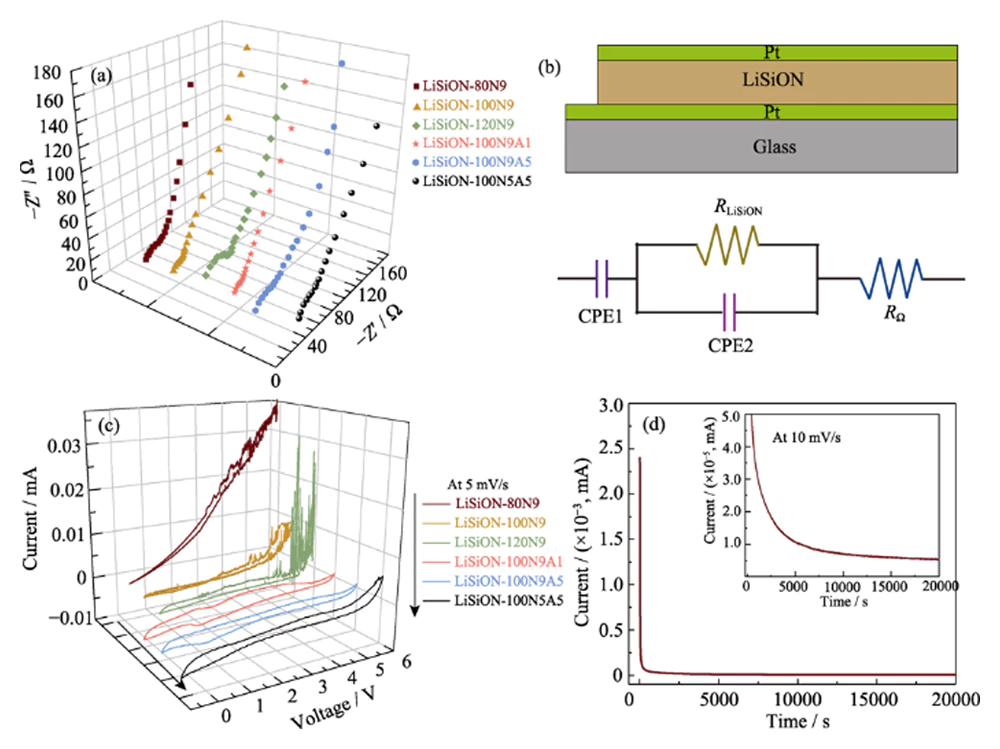
Fig. 3 (a) Espectros de espectroscopia de impedância eletroquímica (EIS) de os filmes finos de LiSiON depositados sob diferentes condições; (b) Esquemático ilustração da estrutura sanduíche Pt/LiSiON/Pt e o correspondente circuito equivalente; (c) Curvas CV dos filmes finos de LiSiON depositados sob condições diferentes; (d) Curva cronoamperométrica da amostra LiSiON-100N9A1
onde d é a espessura do filme, A é a área efetiva (cerca de 1 cm2) e R é a resistência do filme estimada do gráfico de Nyquist medido. As condutividades iônicas calculadas para estes Os filmes finos de LiSiON são comparados na Tabela 1. Conforme observado, a condutividade iônica do filme fino de LiSiON depositado a um fluxo constante de 90 sccm, o N2 aumenta com o aumento da potência de pulverização catódica de 80 W para 100 W, depois diminui quando a potência de pulverização é elevada para 120 W, que é semelhante ao relatório anterior sobre o eletrólito LiPON [18]. Um óbvio incremento nas condutividades iônicas pode ser observado quando a proporção de N2 em o gás de trabalho sob uma potência constante de pulverização catódica de 100 W é promovido, o que pode ser atribuído ao aumento da quantidade de nitrogênio incorporado no LiSiON com ambiente mais favorável para o movimento de íons de lítio[5, 18]. Visivelmente, a amostra LiSiON-100N9 e LiSiON-100N9A1 mostram o maior iônico condutividades de 7,1x10-6 e 6,3x10-6 Sâcm-1, respectivamente, que são obviamente mais altas do que o bem conhecido LiPON (~2×10-6 Sâcm-1), LiNbO3 amorfo relatado anteriormente (~1×10-6 Sâcm-1)[19], LiBON (2,3×10- 6 Sâcm-1)[20], Li-V-Si-O (~1×10-6 Sâcm-1)[21], Li-La-Zr-O (4×10-7 Sâcm-1)[22] e Li-Si-P-O (1,6 × 10-6 Sâcm-1)[23] filmes eletrolíticos, revelando que o amorfo O filme fino LiSiON é um candidato competitivo como eletrólito para TFLB. O alto a condutividade iônica do filme fino LiSiON pode ser atribuída à incorporação de N no filme fino e a formação de ligações Si-N em vez de ligações Si-O, levando a uma rede aniônica mais reticulada para o fácil íon de lítio mobilidade[17, 24]. As janelas de tensão eletroquímica estável do LiSiON filmes finos foram avaliados por medição de CV a uma taxa de varredura de 5 mVâs-1 com tensão de até 5,5 V. Deve-se ressaltar que o impacto da deposição A condição na janela de tensão dos filmes LiSiON varia, o que não pode ser explicado por um mecanismo claro atualmente, uma vez que não existem pesquisas relevantes em relatórios anteriores sobre eletrólito de filme fino [18,24-25]. No entanto, conforme comparado na Fig. 3(c) e Tabela 1, as amostras LiSiON-100N9A1 e LiSiON-100N5A5 mostram a tensão mais ampla janelas de ~ 5,0 e ~ 5,2 V, respectivamente, que são próximas às do LiPON eletrólito. Portanto, tomada tanto a condutividade iônica quanto a janela de tensão em consideração, a amostra LiSiON-100N9A1 foi escolhida para investigação mais aprofundada e a fabricação de célula completa. Para explorar a transferência de íons de lítio número (Ïi) e a condutividade eletrônica (Ïe) da amostra LiSiON-100N9A1, a cronoamperometria foi realizada posteriormente em tensão constante de 10 mV (Fig. 3 (d)). O Ïi pode ser calculado pela Eq. (2).
Ïi=(Ib-Ie)/Ib
onde Ib é a corrente de polarização inicial e Ie é a corrente constante corrente de estado[18]. O Ïi foi calculado como 0,998, que é próximo de 1, indicando que a condução de íons de lítio é absolutamente dominante no eletrólito. O Ïi é determinado por um efeito misto do condução de íons e elétrons [24], que pode ser expressa pela Eq. (3).
Ïi=Ïi/(Ïi+Ïe)
Assim, o Ïe da amostra LiSiON-100N9A1 é calculado como sendo 1,26×10-8 Sâcm-1, que é insignificante em comparação com sua condutividade iônica.
Tabela 1 Comparação de condutividades e tensões de íons de lítio janelas de filmes finos de LiSiON depositados sob diferentes condições
|
Amostra |
Condutividades de íons de lítio |
Tensão |
|
LiSiON-80N9 |
4,6 |
~2,0 |
|
LiSiON-100N9 |
7,1 |
~3,9 |
|
LiSiON-120N9 |
2,5 |
~4,2 |
|
LiSiON-100N9A1 |
6,3 |
~5,0 |
|
LiSiON-100N9A5 |
3,0 |
~4,6 |
|
LiSiON-100N5A5 |
2,9 |
~5,2 |
Para verificar a viabilidade da amostra otimizada LiSiON-100N9A1 para Aplicação TFLB, MoO3/LiSiON/Li TFLB foi posteriormente fabricado. A seção transversal Imagem FESEM e imagens de mapeamento EDS correspondentes do MoO3/LiSiON/Li TFLB são mostrados na Fig. 4(a). Como observado, o cátodo MoO3 (cerca de 1,1 Î1⁄4m de espessura) e o ânodo Li estão bem separados pelo eletrólito LiSiON, e o eletrólito LiSiON tem interfaces de contato firmes com o cátodo e o ânodo. Figura 4(b) exibe a curva CV típica do TFLB a uma taxa de varredura de 0,1 mVâs-1 entre 1,5-3,5 V, que mostra um par de picos redox bem definidos em torno de 2,25 e 2,65 V, correspondendo à inserção e extração de íons de lítio no MoO3[10]. Figura 4(c) representa as 3 curvas iniciais de carga/descarga galvanostática do TFLB em um densidade de corrente de 50 mA-g-1 (20 Î1A-cm-2, com base na massa do filme MoO3). Como observado, o TFLB entrega as capacidades iniciais de carga/descarga de 145/297 mAhâg-1 (58/118,8 μAhcm-2). Após o 2º ciclo, comportamento de ciclo constante com alta reversibilidade capacidade específica de 282 mAhâg-1 foi alcançada pelo TFLB. O desempenho da taxa de o TFLB em várias densidades de corrente é representado na Figura 4 (d). O perda irreversível de capacidade do TFLB em vários ciclos iniciais em baixa corrente a densidade pode ser atribuída à transição de fase irreversível no derivado de MoO3 por inserção de lítio[26]. Capacidades de descarga estáveis de cerca de 219, 173, 107 e 50 mAhâg-1 são observados em 100, 200, 400 e 800 mAâg-1, respectivamente, demonstrando boa capacidade de taxa. Para avaliar a estabilidade eletroquímica do TFLB, o desempenho do ciclo foi ainda realizado a uma densidade de corrente de 200 mAâg-1 (Fig. 4(e)). O TFLB pode reter 78,1% da sua capacidade de descarga inicial após 200 ciclos, e a eficiência coulombiana está próxima de 100% para cada ciclo, revelando aceitável estabilidade eletroquímica do eletrólito LiSiON. As medições EIS foram posteriormente realizado em tensão de circuito aberto para investigar o interface eletrólito/eletrodo no TFLB em diferentes números de ciclo, e o Os gráficos de Nyquist correspondentes com circuito equivalente são representados na Fig. 4 (f). Como observado, o MoO3/LiSiON/Li TFLB mostra um espectro EIS semelhante que consiste de dois semicírculos na região de alta frequência no estado fresco para aquele do MoO3/LiPON/Li TFLB em nosso trabalho anterior[10], indicando que a resistência interfacial Li / LiSiON é insignificante em comparação com a do Interface LiSiON/MoO3[20]. O primeiro pequeno semicírculo nas parcelas de Nyquist é atribuído à condução iônica de íons Li + no eletrólito LiSiON, enquanto o segundo grande semicírculo corresponde ao processo de transferência de carga no Interface LiSiON/MoO3 [27,28]. Nota-se que o primeiro semicírculo pequeno raramente mudanças durante os ciclos, indicando a estabilidade cíclica relativamente boa de o eletrólito LiSiON. No entanto, o segundo semicírculo se expande gradualmente à medida que o o número do ciclo evolui, revelando o aumento da interface LiSiON/MoO3 resistência durante o ciclismo, o que pode ser a principal razão para a capacidade desvanecimento do TFLB[29]. Vale ressaltar que este trabalho teve sucesso adota o eletrólito LiSiON para construir TFLB e demonstra o bom contato interfacial de LiSiON com o cátodo MoO3 e o ânodo de lítio para o primeira vez. Além disso, a grande capacidade específica, boa capacidade de taxa e desempenho de ciclo aceitável do MoO3/LiSiON/Li TFLB demonstra que o LiSiON filme fino é bem aplicável como eletrólito para TFLB.
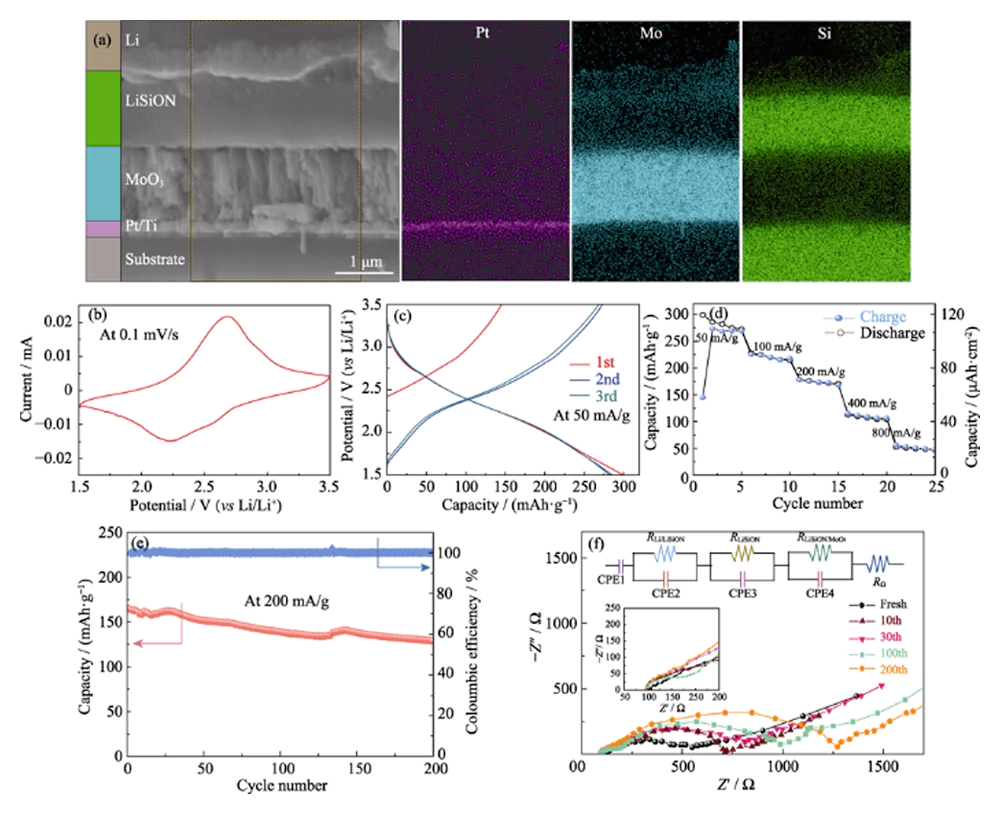
Fig. 4 (a) Imagem FESEM de seção transversal e mapeamento EDS correspondente imagens do MoO3/LiSiON/Li TFLB; (b) Curva CV típica, (c) três curvas iniciais de carga/descarga, (d) taxa desempenho, (e) desempenho do ciclo e (f) espectros EIS em diferentes ciclos números do MoO3/LiSiON/Li TFLB com amostra LiSiON-100N9A1 como eletrólito
3 Conclusões
Em resumo, o eletrólito de filme fino LiSiON amorfo foi com sucesso preparado por pulverização catódica de RF usando alvo de Li2SiO3 com fluxo de gás N2/Ar. O filme fino LiSiON otimizado depositado sob potência de RF de 100 W no fluxo de 90 sccm N2 e 10 sccm Ar possuem superfície lisa, estrutura densa, alto teor de íons condutividade (6,3×10-6 Sâcm-1) e ampla janela de tensão (5 V), tornando-o um promissor material eletrolítico para TFLB. Mais importante ainda, usando o LiSiON eletrólito, um MoO3/LiSiON/Li TFLB foi demonstrado com sucesso para o primeira vez com alta capacidade específica (282 mAhâg-1 a 50 mAâg-1), bom desempenho de taxa (50 mAhâg-1 a 800 mAâg-1) e estabilidade de ciclo aceitável (78,1% de retenção de capacidade após 200 ciclos). Espera-se que este trabalho traga novas oportunidades para desenvolver desempenho TFLB usando eletrólito de filme fino à base de Li2O-SiO2.
Referências
[1] MOITZHEIM S, PUT B, VEREECKEN P M. Avanços em baterias de íon-lítio de película fina 3D. Interfaces de materiais avançados, 2019,6(15):1900805.
[2] XIA Q, ZHANG Q, SUN S, et al. Matrizes de nanofolhas LixMnO2 de intercrescimento em túnel como cátodo 3D para microbaterias de lítio de filme fino de estado sólido de alto desempenho. Materiais Avançados, 2021,33(5):2003524.
[3] DENG Y, EAMES C, FLEUTOT B, et al. Aumentando a condutividade de íons de lítio em eletrólitos sólidos de condutores superiônicos de lítio (LISICON) por meio de um efeito poliânion misto. Materiais Aplicados e Interfaces ACS, 2017,9(8):7050-7058.
[4] BATES JB, DUDNEY NJ, GRUZALSKI GR, et al. Fabricação e caracterização de filmes finos de eletrólito de lítio amorfo e baterias recarregáveis de filme fino. Jornal de Fontes de Energia, 1993,43(1/2/3):103-110.
[5] BATES J. Propriedades elétricas de filmes finos de eletrólito de lítio amorfo. Solid State Ionics, 1992,53(56):647-654.
[6] FAMPRIKIS T, GALIPAUD J, CLEMENS O, et al. Dependência da composição da condutividade iônica em eletrólitos de filme fino LiSiPO (N) para baterias de estado sólido. Materiais Energéticos Aplicados ACS, 2019,2(7):4782-4791.
[7] DENG Y, EAMES C, CHOTARD JN, et al. Insights estruturais e mecanísticos sobre a condução rápida de íons de lítio em eletrólitos sólidos Li4SiO4-Li3PO4. Jornal da Sociedade Americana de Química, 2015,137(28):9136-9145.
[8] CHEN R, SONG X. A condutividade iônica de eletrólitos sólidos para sistemas Li4+xMxSi1-xO4-yLi2O (M=Al, B). Jornal da Sociedade Química Chinesa, 2002,49:7-10.
[9] ADNAN S, MOHAMED N S. Efeitos da substituição de Sn nas propriedades do eletrólito cerâmico Li4SiO4. Iônicos de Estado Sólido, 2014,262:559-562.
[10] SUN S, XIA Q, LIU J, et al. Matrizes autônomas de nanoflocos α-MoO3-x com deficiência de oxigênio como cátodo 3D para baterias avançadas de lítio de película fina totalmente em estado sólido. Journal of Materiomics, 2019,5(2):229-236.
[11] DING W, LU W, DENG X, et al. Um estudo XPS sobre a estrutura do filme SiNx depositado por pulverização catódica de magnetron ECR por microondas. Acta Physica Sinica, 2009,58(6):4109-4116.
[12] KIM H, KIM Y. Nitretação parcial de Li4SiO4 e condutividade iônica de Li4. 1SiO3. 9N0. 1Ceramics International, 2018,44(8):9058-9062.
[13] MARIKO M, HIDEMASA K, TOMOYUKI O, et al. Análise de ânodos de SiO para baterias de íon-lítio. Jornal da Sociedade Eletroquímica, 2005,152(10):A2089.
[14] FINGERLE M, BUCHHEIT R, SICOLO S, et al. Reação e formação de camada de carga espacial na interface LiCoO2-LiPON: insights sobre a formação de defeitos e alinhamento do nível de energia iônica por uma abordagem combinada de simulação científica de superfície. Materiais Químicos, 2017,29(18):7675-7685.
[15] WEST W, HOOD Z, ADHIKARI S, et al. Redução da resistência à transferência de carga na interface eletrólito-eletrodo sólido por deposição de filmes a laser pulsado de uma fonte cristalina de Li2PO2N. Jornal de Fontes de Energia, 2016,312:116-122.
[16] SICOLO S, FINGERLE M, HAUSBRAND R, et al. Instabilidade interfacial de LiPON amorfo contra lítio: uma teoria funcional de densidade combinada e estudo espectroscópico. Jornal de Fontes de Energia, 2017,354:124-133.
[17] WU F, LIU Y, CHEN R, et al. Preparação e desempenho de novo eletrólito de filme fino Li-Ti-Si-P-O-N para baterias de lítio de filme fino. Jornal de Fontes de Energia, 2009,189(1):467-470.
[18] PUT B, VEREECKEN M, MEERSSCHAUT J, et al. Caracterização elétrica de camadas ultrafinas de LiPON pulverizadas por RF para baterias em nanoescala. Materiais Aplicados e Interfaces ACS, 2016,8(11):7060-7069.
[19] NIINOMI H, MOTOYAMA M, IRIYAMA Y. Condução de Li+ em filmes de Li-Nb-O depositados por um método Sol-Gel. Iônico de Estado Sólido, 2016,285:13-18.
[20] SONG S, LEE K, PARK H. Microbaterias flexíveis de alto desempenho totalmente em estado sólido baseadas em eletrólito sólido de oxinitreto de boro e lítio. Jornal de Fontes de Energia, 2016,328:311-317.
[21] OHTSUKA H, OKADA S, YAMAKI J. Bateria de estado sólido com filme fino de eletrólito sólido Li2O-V2O5-SiO2. Solid State Ionics, 1990,40-41:964-966.
[22] Kalita D, Lee S, Lee K, et al. Propriedades de condutividade iônica do eletrólito sólido amorfo Li-La-Zr-O para baterias de película fina. Iônico de Estado Sólido, 2012,229:14-19.
[23] SAKURAI Y, SAKUDA A, HAYASHI A, et al. Preparação de filmes finos amorfos de Li4SiO4-Li3PO4 por deposição a laser pulsado para baterias secundárias de lítio totalmente em estado sólido. Iônico de Estado Sólido, 2011,182:59-63.
[24] TAN G, WU F, LI L, et al. Preparação de pulverização catódica magnetron de eletrólitos de filme fino à base de fosfato de lítio-alumínio-titânio incorporados com nitrogênio para baterias de íon de lítio totalmente em estado sólido. The Journal of Physical Chemistry C, 2012,116(5):3817-3826.
[25] YU X, BATES JB, JELLISON G, et al. Um eletrólito de lítio de película fina estável: oxinitreto de fósforo e lítio. Jornal da Sociedade Eletroquímica, 1997,144(2):524.
[26] KIM H, COOK J, LIN H, et al. As vagas de oxigênio melhoram as propriedades de armazenamento de carga pseudocapacitiva do MoO3-x. Materiais da Natureza, 2017,16:454-460.
[27] SONG H, WANG S, SONG X, et al. Baterias de lítio-ar movidas a energia solar, totalmente em estado sólido, operando em temperaturas extremamente baixas. Energia e Ciência Ambiental, 2020,13(4):1205-1211.
[28] WANG Z, LEE J, XIN H, et al. Efeitos da camada interfacial de eletrólito catódico (CEI) no ciclo de longo prazo de baterias de película fina totalmente de estado sólido. Jornal de Fontes de Energia, 2016,324:342-348.
[29] QIAO Y, DENG H, HE P, et al. Uma célula de lítio-metal de 500 Wh/kg baseada em redox aniônico. Joule, 2020,4(6):1311-1323.