Categorias
novo blog
- Comparação de materiais catódicos para baterias: NMC vs LFP vs NCA
- Tendências de fabricação de baterias de íon-lítio até 2026: um guia para compradores B2B
- Guia passo a passo do processo de fabricação de baterias de íon-lítio
- Principais causas de vazamento na selagem das células da bolsa
- Formação e classificação na fabricação de baterias de íon-lítio
Tags
Sb dopado tipo O3 Na0.9Ni0.5Mn0.3Ti0.2O2 Material de cátodo para bateria de íons de Na
Material de cátodo dopado com O3 tipo Na0.9Ni0.5Mn0.3Ti0.2O2 para bateria de íon-Na
KONG Guoqiang, LENG Mingzhe, ZHOU Zhanrong, XIA Chi, SHEN Xiaofang. Cátodo dopado com O3 tipo Na0.9Ni0.5Mn0.3Ti0.2O2 Sb Material para bateria de íon Na[J]. Jornal de Materiais Inorgânicos, 2023, 38(6): 656-662.
Resumo
Estabilidade do ciclo e capacidade específica de materiais catódicos para baterias de íon de sódio desempenham um papel importante na obtenção sua ampla aplicação. Com base na estratégia de introdução de heteroelementos para otimizar a estabilidade estrutural e capacidade específica de materiais catódicos, O3-Na0,9Ni0,5-xMn0,3Ti0,2SbxO2 (NMTSbx, x=0, 0,02, 0,04, 0,06) foi preparado por um método simples de reação no estado sólido, e os efeitos do Sb quantidade de dopagem nas propriedades de armazenamento de sódio de Na0,9Ni0,5Mn0,3Ti0,2O2 materiais catódicos foram investigados. Os resultados da caracterização mostram que o força de repulsão eletrostática entre átomos de oxigênio no metal de transição camada é reduzida após a dopagem com Sb, enquanto o espaçamento da rede é expandido, o que é propício à desintercalação de Na+. Enquanto isso, o elétron forte a deslocalização causada pela dopagem com Sb diminui a energia de todo o sistema, levando a uma estrutura estável, mais propícia ao carregamento cíclico e descarregando. O teste eletroquímico mostra que a descarga inicial específica a capacidade do NMTSb0 não dopado é de 122,8 mAh · g · 1 a 1C (240 mA · g · 1), e a taxa de retenção de capacidade é de apenas 41,5% após 200 ciclos. Mas a capacidade específica de descarga inicial do NMTSb0.04 dopado é de 135,2 mAh · g · 1 a 1C, e a taxa de retenção de capacidade é de até 70% após 200 ciclos. Este estudo mostra que o cátodo O3 dopado com Sb tipo Na0.9Ni0.5Mn0.3Ti0.2O2 material pode melhorar significativamente a capacidade específica de descarga inicial e taxa de retenção de capacidade das baterias de íon de sódio. Nossos resultados sugerem que Sb estratégia de doping pode ser uma abordagem útil para a preparação de alta estabilidade baterias de íon de sódio.
Palavras-chaveï¼ Sb dopagem; Tipo O3; material catódico; método de fase sólida; ampla tensão; Íon Na fabricação de baterias
Desde a comercialização de íons de lítio baterias, elas têm sido amplamente utilizadas em dispositivos eletrônicos portáteis, elétricos veículos e armazenamento de energia eletroquímica, etc. No entanto, o limitado recursos e a distribuição desigual de lítio é um fator importante que restringe o desenvolvimento de baterias de íon-lítio. Ao mesmo tempo, as reservas de sódio são abundante e amplamente distribuído e, mais importante, devido à semelhança de as propriedades químicas do lítio e do sódio, o princípio de funcionamento do as baterias de íon de sódio são próximas às baterias de íon de lítio. Portanto, o aplicação de baterias de íon de sódio na área de armazenamento de energia em grande escala recebeu grande atenção.
Materiais catódicos para baterias de íon de sódio
incluem principalmente óxidos em camadas de metais de transição, compostos polianiônicos e
Análogos do azul da Prússia. Entre eles, o óxido em camadas NaxTMO2 (TM refere-se a
metal de transição, 0
Entre os vários materiais NaxTMO2 do tipo O3 que foram relatados, NaxTMO2 contendo Ni e Mn atraiu muitos atenção devido aos seus abundantes recursos de Ni/Mn e alta capacidade de armazenamento. Por exemplo, NaNi0,5Mn0,5O2 do tipo O3 tem uma alta capacidade reversível (133mAh gâ1). Bom desempenho de taxa (30C, 40mAh gâ1) e ciclo de vida longo (retenção de capacidade específica de 70% após 500 ciclos a 3,75C). No entanto, ainda existem alguns problemas que restringem a sua posterior desenvolvimento, como desempenho de taxa insatisfatória, transição de fase complexa durante a carga e descarga, e rápida queda de capacidade, especialmente em altas tensões de 4,1-4,5 V. Estudos recentes mostraram que a dopagem parcial de outros elementos podem efetivamente melhorar a reversibilidade da transição de fase. Para exemplo, Na0.9Ni0.4Mn0.4Ti0.2O2 dopado com Ti tem uma fase O3-P3 mais reversível transição entre 2,5 e 4,2 V, maior capacidade específica (197 mAh g-1), e desempenho de ciclo mais estável. NaFe0.2Mn0.4Ni0.4O2 dopado com Fe tem um alto capacidade reversível (165 mAh g-1) e uma transição de fase estável (87% da capacidade retenção após 200 ciclos) na faixa de 4,0-4,3 V.
Além disso, o doping Sb5+ também pode melhorar a estabilidade do ciclo e a tensão de trabalho dos materiais catódicos. A fim de obter uma estrutura de material mais estável e desempenho de taxa superior em um faixa de tensão mais ampla para óxidos em camadas do tipo O3. Neste estudo, o Sb5+ foi parcialmente substituído por Ni2+ em Na0,9Ni0,5Mn0,3Ti0,2O2 (NMT) por um simples método de estado sólido para estudar o efeito da dopagem com Sb na eletroquímica desempenho de óxidos em camadas e a mudança de reversibilidade da fase O3-P3 transição em uma ampla faixa de tensão.
1 Método experimental
1.1 Preparação do material
Na0,9Ni0,5-xMn0,3Ti0,2SbxO2 (NMTSbx, x=0, 0,02, 0,04, 0,06) materiais foram preparados pelo método de fase sólida. O específico as etapas são as seguintes: misture Na2CO3, NiO, Sb2O5, MnO2 e TiO2 no proporção estequiométrica correspondente e adicione uma fração molar adicional de 5% de Na2CO3 considerando a volatilidade do Na em alta temperatura. Moa uniformemente com um almofariz de ágata e use uma máquina de comprimidos para fazer um disco fino de Ï16 mm. Tratamento térmico a 950 °C em atmosfera de ar duas vezes, de cada vez por 12h. O mesmo procedimento foi usado para preparar NMTSb0 sem Sb2O5 iniciando material, e todas as amostras foram armazenadas em um porta-luvas para uso futuro.
1.2 Conjunto de Bateria
O material ativo NMTSbx, negro de acetileno e fluoreto de polivinilideno (PVDF) foram pesados na proporção de massa de 7:2:1, e uma quantidade apropriada de N-metilpirrolidona (NMP) foi adicionada para moer para obter uma pasta uniformemente misturada. A pasta foi revestida na superfície de alumínio folha, e a carga superficial do material ativo no eletrodo foi de cerca de 2,5 mg cm-2. Seco a vácuo a 80°C durante 12 h e depois cortado em pequenos discos de Ï12 mm com um micrótomo como eléctrodo positivo. Botão CR2032 as células foram montadas em um porta-luvas cheio de gás Ar (as frações volumétricas de água e oxigênio foram ambos inferiores a 1×10-6). Entre eles, o contraeletrodo é uma folha de metal de sódio, o separador é de fibra de vidro e o eletrólito é 1 mol L-1 NaClO4 carbonato de dibutila + solução de carbonato de fluoroetileno (volume proporção 1: 1).
1.3 Caracterização e testes de materiais
O espectro de difração de raios X (XRD) do amostra foi testada usando MiniFlex 600 (Rigaku, Japão, Cu Kα), e o cristal estrutura foi posteriormente refinada por Rietveld através da análise estrutural sistema (GSAS + EXPGUI). A morfologia microscópica e o tamanho das partículas do amostras foram observadas por microscópio eletrônico de varredura JSM-7610F (JEOL, Japão) (SEM) e microscópio eletrônico de transmissão de alta resolução JEOL JEM-2100F (HRTEM). A espectroscopia de fotoelétrons de raios X (XPS) do estado de valência do elementos foram testados em um espectrômetro Escalab250xi usando raios X acromáticos AlKα fonte. A razão molar de cada elemento da amostra foi analisada por espectrômetro de emissão óptica com plasma indutivamente acoplado (ICP-AES, iCAP 6300). As medições de carga e descarga foram realizadas à temperatura ambiente usando um Sistema de teste de bateria Land CT2001A entre 2,0 e 4,2 V, e o eletroquímico espectroscopia de impedância (EIS) dos eletrodos foi medida usando um CHI660E estação de trabalho eletroquímica (CH Instruments).
2 Resultados e discussão
2.1 Características estruturais do NMTSbx
A composição elementar de todas as amostras foi determinado pelo ICP-AES, e os resultados são mostrados na Tabela S1. Dentro do faixa de erro de medição, o conteúdo real de cada íon metálico é basicamente consistente com a composição do projeto. No espectro de XRD da Fig. 1 (a), todos as amostras têm estrutura α-NaFeO2 hexagonal do tipo O3 (grupo espacial R-3m), consistente com NaNi0,5Mn0,5O2 (JCPDS 54-0887). É mostrado que o a introdução de Sb na rede NMT não altera a estrutura intrínseca do material. O processo de preparação de cátodos de óxido com alto teor de níquel por o método de estado sólido produzirá inevitavelmente uma pequena quantidade de resíduo componentes inativos de NiO, e a literatura mostra que o impacto de vestígios quantidades de NiO no desempenho da bateria são insignificantes. Na Figura 1 (b), o picos de difração de NMTSb0,02, NMTSb0,04 e NMTSb0,06 mudaram para grandes ângulos, e picos diversos começaram a aparecer em NMTSb0,06. De acordo com o Equação de Bragg (nλ=2dsinθ), o tamanho médio do grão do pó é qualitativamente analisado. onde n é a ordem de difração, d é a espessura média (nm) dos grãos da amostra perpendiculares à direção do cristal plano, θ é o ângulo de difração correspondente à difração mais forte pico e λ é o comprimento de onda dos raios X (nm). Os resultados do cálculo do plano de cristal mostram que o tamanho do grão da amostra diminui após a dopagem com Sb, o que é relacionado à diferença no raio iônico de Sb (0,06 nm) e Ni (0,069 nm). De acordo com o teorema de Vegard, isto também significa que uma solução sólida reação ocorreu durante a formação de NMTSbx.
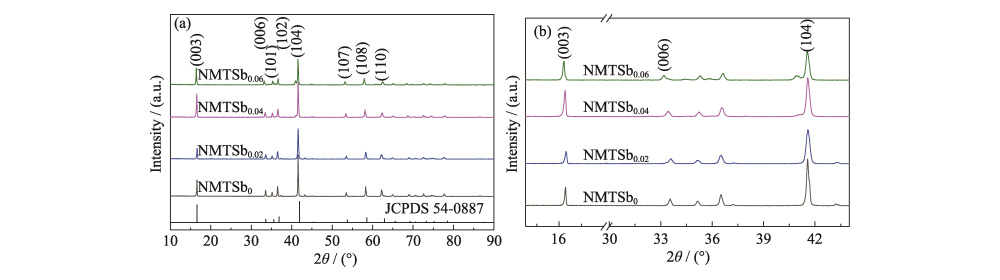
Fig. 1 Pesquisa (a) e ampliados (b) padrões de XRD de NMTSbx (x = 0, 0,02, 0,04, 0,06)
A Figura 2 (a, b) mostra o XRD refinado Padrões Rietveld de NMTSb0 e NMTSb0.04 e os parâmetros de rede detalhados são mostrados na Tabela S2. Pode-se ver que os parâmetros de rede de NMTSb0.04 (a = b = 0,29790 nm) são ligeiramente reduzidos em comparação com o NMTSb0 original (a=b=0,29812 nm). Isto também é atribuído ao fato de que o raio iônico do Sb (0,06 nm) é menor que o do Ni (0,069 nm), o que é consistente com o Análise de DRX. O c (c = 1,608391 nm) de NMTSb0,04 foi aumentado em comparação com o de NMTSb0 (c = 1,600487 nm). A principal razão é que o parâmetro de rede a/b é sensível à mudança do comprimento da ligação (Ni/Mn/Ti/Sb)-O do plano basal da estrutura em camadas, e a incorporação de Sb encurta a ligação comprimento. Isso causa a repulsão eletrostática entre os átomos de oxigênio no camada contínua de metal de transição (Ni/Mn/Ti/Sb) se torne maior, levando a um aumento em c. Além disso, após o cálculo, o c/a de NMTSb0 e NMTSb0.04 fez não mudaram muito, foram 5,36 e 5,39 respectivamente, ambos foram maiores que 4,99, indicando que as amostras dopadas mantiveram uma boa estrutura em camadas.
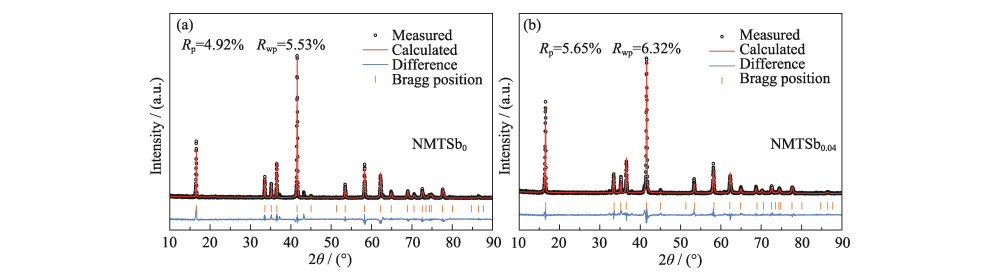
Fig. 2 Rietveld padrões de XRD de refinamento de NMTSb0 (a) e NMTSb0.04(b)
A Figura 3 mostra as imagens SEM de NMTSb0 e NMTSb0,04. Ambos os produtos são compostos por um grande número de micro-nano-escala discos finos com espessura uniforme e bordas claras. Especialmente depois do doping do Sb, a superfície do floco é mais lisa e não faltam flocos hexagonais estrutura com arestas e cantos afiados. Análise elementar EDS de área selecionada de NMTSb0.04 mostra que os elementos Na, O, Ni, Ti, Mn e Sb estão distribuídos uniformemente na amostra, o que também prova que os elementos Sb foram dopados com sucesso em a estrutura intrínseca de NMTSb0.

Fig. 3 SEM imagens e mapeamentos EDS de NMTSb0 (a, b) e NMTSb0.04 (c, d)
As microestruturas de NMTSb0 e NMTSb0.04 foram posteriormente observados pelo HRTEM, e os resultados são mostrados na Figura S1. Em Figura S1 (a, c), as partículas antes e depois da dopagem com Sb estão conectadas ou sobrepostos e macroscopicamente aparecem como uma folha ou aproximadamente estrutura circular ou poligonal. As imagens HRTEM da Figura S1 (b, d) mostram o franjas de rede do material e os espaçamentos de rede de NMTSb0 e NMTSb0,04 são 0,238 e 0,237 nm, respectivamente. Ambos correspondem ao (101) plano de cristal, e o efeito da dopagem Sb no espaçamento da rede é consistente com os resultados da análise XRD. As inserções da Figura S1 (b, d) são os pontos de o padrão de difração de elétrons de área selecionada (SEAD) de NMTSb0 e NMTSb0,04, o que prova que os NMTSb0 e NMTSb0.04 obtidos apresentam boa cristalinidade.
A espectroscopia de fotoelétrons de raios X (XPS) da Figura S2 mostra os resultados do estado de oxidação dos elementos Mn, Ni, Ti e Sb em NMTSb0 e NMTSb0,04. Na Figura S2 (a), os dois picos principais de NMTSb0 em 877 e 850 eV correspondem a Ni2p1/2 e Ni2p3/2, respectivamente, e ambos pertencem a Ni2+ na amostra. O pico de energia de ligação em 858,2 eV é um satélite comum pico no elemento Ni. O Ni2p1/2 de NMTSb0.04 se divide em dois picos, indicando que a introdução de Sb na rede NMTSb0 pode reduzir o número de elétrons externos em torno do Ni, resultando em uma forte deslocalização de elétrons efeito. Os metais de transição têm orbitais d mais deslocalizados, o que pode melhorar a interação metal-metal dos octaedros de compartilhamento lateral MO6 nas camadas estrutura, inibindo assim o colapso dos octaedros MO6 e aliviando as reações colaterais do oxigênio da rede e do eletrólito. Durante o processo de carga-descarga, a estrutura do material de óxido em camadas torna-se mais estável, indicando que a forte deslocalização de elétrons é benéfica para a estabilidade estrutural de NMTSb0.04. Para o elemento Mn, o pico Mn2p3/2 em 642 eV e o pico Mn2p1/2 em 652 eV na Figura S2 (b) indicam a presença de Mn no estado de valência +4 em NMTSb0 e NMTSb0,04. O pico Mn2p3/2 em 643eV pode ser combinado com o pico Mn3+. A configuração octaédrica do Mn3+ ficará deformado, o que é causado pela distorção de Ginger-Taylor. A dissolução do elemento Mn levará a um rápido declínio na capacidade, enquanto Ti em NMTSb0.04 substitui parte do Mn, e a redução do teor de Mn também pode estabilizar o estrutura estrutural do material, inibindo assim o rápido declínio da capacidade da bateria causada pelo efeito gengibre-Taylor. A energia de ligação típica picos de Ti2p1/2 e Ti2p3/2 em 457,3 e 453,1 eV para NMTSb0 na Figura S2 (c) correspondem ao estado de valência estável +4 do Ti. Enquanto o Ti2p1/2 e Ti2p3/2 picos em 454,1 e 463,9 eV de NMTSb0,04 correspondem a Ti na valência +3 estado. Do ponto de vista da compensação de encargos, isto se deve principalmente ao reação de redução do Ti após a introdução do Sb5+ de alta valência. Durante Após a reação carga-descarga, o Ti4+ continuou a existir em uma forma estável, o que foi verificado na curva de voltametria cíclica (CV) de NMTSb0,04, conforme mostrado em Figura 4. Isso também mostra que a fonte da capacidade da bateria não tem nada a ver com o par redox Ti4+/Ti3+. Além disso, os picos de energia de ligação NMTSb0,04 a 529-536 eV na Figura S2 (d) confirma a presença de Sb.
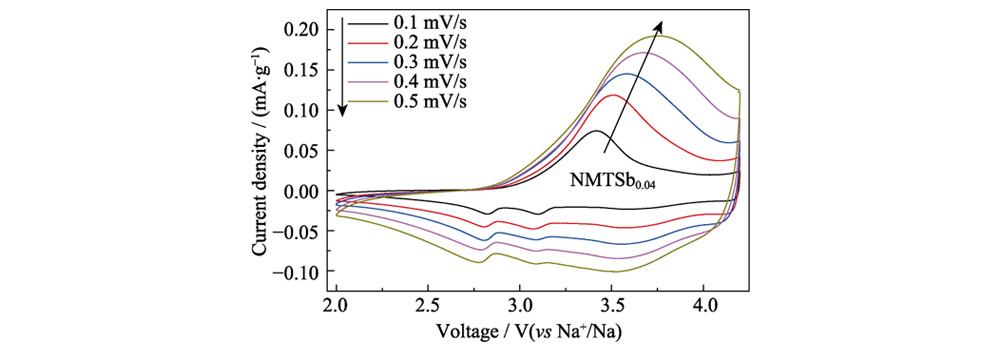
Fig. 4 CV curvas de material catódico NMTSb0.04
2.2 Desempenho eletroquímico
A Figura 5 mostra o eletroquímico gráfico de Nyquist de impedância de NMTSbx. Entre eles, o semicírculo no meio e região de alta frequência representa a resistência à transferência de carga (Rct) entre o eletrólito e o eletrodo, e a linha oblíqua na baixa frequência região representa a resistência de Warburg causada pela difusão de sódio íons. Ajustar o circuito equivalente mostra que o Rct de NMTSb0 e NMTSb0.04 são 1185,4 e 761 Ω, respectivamente. À medida que o conteúdo de doping Sb aumenta, o a impedância da amostra também diminui. Quando x=0,04, a impedância do amostra atinge o valor mínimo. Aumentando ainda mais o conteúdo de doping Sb leva a um aumento na impedância. Quando x = 0,06, a impedância excede a de a amostra NMTSb0. O conteúdo apropriado de dopagem pode obter o metal ideal espaçamento entre camadas da estrutura em camadas, garante transporte suave de elétrons canais, ajudam a melhorar as características dinâmicas de NMTSb0.04, e no ao mesmo tempo, leve em consideração a estabilidade da estrutura geral.
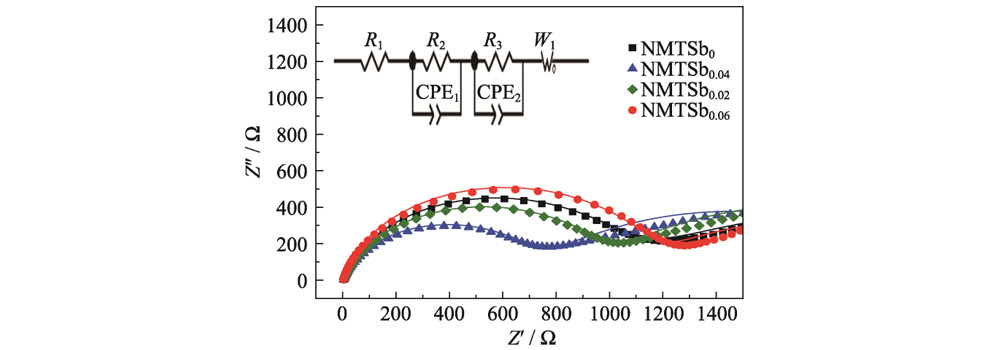
Fig. 5 Eletroquímica espectros de impedância de NMTSbx
Sob a condição de densidade de corrente de 1C (240 mA·gâ1) e faixa de tensão de 2,0-4,2 V, o sódio desempenho de armazenamento da bateria de íons de Na com NMTSbx como o eletrodo foi testado. Conforme mostrado na Figura 6 (a), as capacidades reversíveis de NMTSbx (x = 0, 0,02, 0,04, 0,06) as amostras são 122,8, 128,0, 135,2 e 103,9 mAh g-1, respectivamente. A diferença na capacidade específica se deve a diferentes conteúdos de dopagem. A estratégia de substituição de elementos químicos pode suprimir a transição de fase irreversível e melhorar o transporte de íons de sódio cinética. As vantagens são resumidas da seguinte forma: substituir altamente ativos elementos com elementos eletroquimicamente inativos e estruturalmente estáveis, tais como prevenir a mistura de cátions, aumentando a barreira energética da migração de Ni2+, e reduzindo o oxigênio liberado durante o ciclo eletroquímico por fortalecimento das ligações metal-oxigênio. Dopagem ou substituição de sítios de metais de transição pode inibir significativamente a transição de fase, inibir íons metálicos de transição migração e melhorar a estabilidade química e eletroquímica de materiais dessódicos. O conteúdo específico de doping deve ser explorado de acordo com o tipo de elemento dopante e a estrutura intrínseca. . No por um lado, a dopagem com íons metálicos de alta valência pode melhorar a condutividade em massa do material depois que os íons metálicos entram no interior da rede. Quando a fração molar de dopagem é superior a 1% (razão estequiométrica x0,01), a resistividade diminuirá rapidamente, o que terá um grande influência na condutividade. Por outro lado, uma quantidade demasiado elevada de dopagem inevitavelmente reduzem o conteúdo de pares redox no sistema e afetam o densidade de energia do sistema, embora uma quantidade muito pequena de dopagem não seja suficiente para estabilizar a estrutura de materiais de óxido em camadas. Neste estudo, NMTSbx(x=0, 0,02, 0,04, 0,06), x é a razão estequiométrica e o valor real o conteúdo de dopagem é de 2%, 4% e 6% por fração molar, respectivamente.
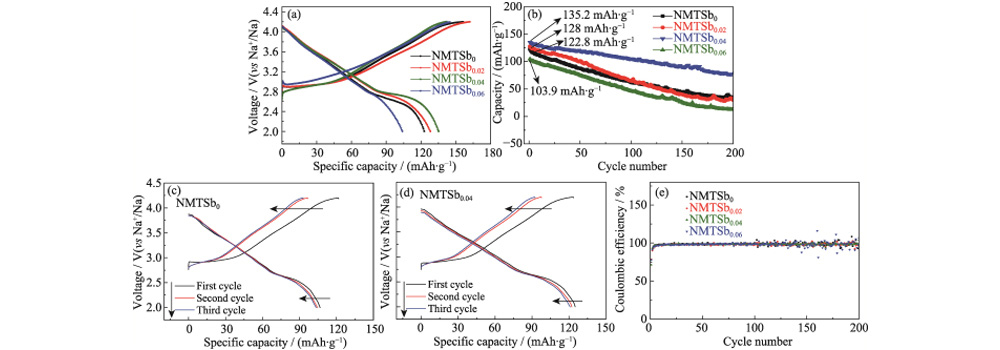
Fig. 6 Desempenho de baterias de íon Na com NMTSbx como eletrodos
(a) Carregamento e curvas de descarga de baterias de íon Na com amostras como eletrodos para o primeiro ciclo a 1C; (b) Desempenho de ciclagem de baterias de íons de Na com amostras como eletrodos a 1C por 200 ciclos; (c, d) Carregamento e descarregamento curvas de baterias de íon Na com amostras como eletrodos para 3 ciclos iniciais a 5C; (e) Eficiências Coulombic de baterias de íon Na com NMTSbx como eletrodos para 200 ciclos a 1C Figuras coloridas estão disponíveis em site
Na Fig. 6 (a), a curva de carga-descarga de a amostra não dopada NMTSb0 obviamente contém múltiplos platôs de tensão e etapas, indicando que múltiplas transições de fase de hexagonal para monoclínica pode ocorrer na estrutura em camadas. No entanto, embora o deslizamento intercalar do ocorre uma camada de metal de transição, a curva geral de carga-descarga é relativamente suave. As três plataformas de tensão acima de 3,00 V tendem a ficar confusas. Para NMTSb0, a curva de carga é dividida principalmente em duas partes: a seção de inclinação em torno de 3,00-3,80 V e a longa seção do platô acima de 3,80 V. No entanto, quando Sb foi introduzido, a tensão inicial do segmento da plataforma aumentou acima 4,00 V. Para a curva de descarga, o longo platô geralmente ocorre na tensão faixa de 2,50-2,75 V. A aparência do platô de tensão pode ser atribuída à transformação da fase O3 na fase P3, enquanto a inclinação segmento quando a tensão aumenta é causada pela reação da solução sólida com a estrutura P3. A Figura 6 (b) é uma comparação do desempenho do ciclo de Eletrodos NMTSbx (x=0, 0,02, 0,04, 0,06) a uma densidade de corrente de 1C. Isso é vale a pena notar que a estabilidade do ciclo do material catódico NMTSb0.04 é a melhor, e cerca de 70% da capacidade reversível pode ser retida após 200 ciclos. Em contraste, a capacidade específica do eletrodo NMTSb0 decai muito rapidamente, com valor inicial de 122,8 mAh g-1, que cai para 51 mAh g-1 após 200 ciclos, restando apenas 41,5% da capacidade específica. Na Figura 6 (c, d), mesmo a uma taxa muito alta de 5C (1200 mA gâ1), o a retenção da capacidade específica do eletrodo NMTSb0,04 ainda é de 92,6% (125,3 mAh gâ1). A capacidade específica do NMTSb0 eletrodo é de apenas 106,7 mAh·gâ1, o que é superior ao outros óxidos em camadas do tipo O3 relatados. A capacidade específica de descarga inicial de O3-Na(Ni1/3Mn1/3Fe1/3)0,95Al0,05O2 preparado pelo grupo de Yan a uma taxa de 0,1C é 145,4 mAh · g · 1. E depois de 80 ciclos a uma taxa de 0,2C, o específico reversível a capacidade é de 128,4 mAh·gâ1. O3-NaNi0,5Mn0,5O2 elaborado pelo grupo de pesquisa de Guo tem capacidade específica de 80 mAh·g-1 na faixa de tensão de 2-4 V a uma taxa de 2C. A Figura 6 (e) apresenta a eficiência coulombiana do Bateria de íon Na durante ciclo contínuo a 1C. Entre eles, o Coulombic distribuição de eficiência do eletrodo NMTSb0.04 é estável e tende a um linha reta, mantendo-se basicamente em 98%, o que também indica que seu a estrutura em camadas é mais estável. No entanto, a eficiência coulombiana do O eletrodo NMTSb0 flutuou significativamente após 140 ciclos, e houve um grande salto quando estava perto de 200 ciclos. A bateria montada com NMTSb0,04 após 200 ciclos foi desmontado e processado, e o espectro de XRD da folha de eletrodo foi testada, os resultados são mostrados na Figura S3. O XRD os picos de difração da peça polar NMTSb0.04 não mudaram significativamente após ciclagem, indicando que a mudança de fase irreversível do cátodo NMTSb0.04 material foi suprimido após doping.
3 Conclusão
Neste estudo, Na0,9Ni0,5-xMn0,3Ti0,2SbxO2 (NMTSbx, x = 0, 0,02, 0,04, 0,06), um material de cátodo de óxido em camadas para baterias de íon de sódio, foi preparado por um método conveniente de estado sólido. Isso é partículas são compostas de flocos em escala micro-nano com espessura uniforme e bordas claras, e o tamanho do grão diminui depois que o Sb substitui parte do Ni. No ao mesmo tempo, a dopagem de Sb causa forte deslocalização de elétrons, o que reduz a energia de todo o sistema e obtém uma estrutura estável que é mais propício para ciclos de carga-descarga de longo prazo. Na eletroquímica teste na faixa de 2,00-4,20 V, a dopagem de Sb suprimiu a fase irreversível transição do material catódico e melhorou a plataforma de tensão de trabalho. Quando carregado e descarregado a uma taxa de 1C, a capacidade específica de descarga inicial de NMTSb0,04 é 135,2 mAh·g-1, e a taxa de retenção de capacidade após 200 ciclos é 70%. A retenção de capacidade específica pode atingir 92,6% (125,3 mAh·gâ1) a uma taxa de 5C.
Informações Complementares

Fig. S1 HRTEM imagens de NMT (a, b) e NMTSb0.04 (c, d) com inserção em (b, d) mostrando imagens SEAD correspondentes
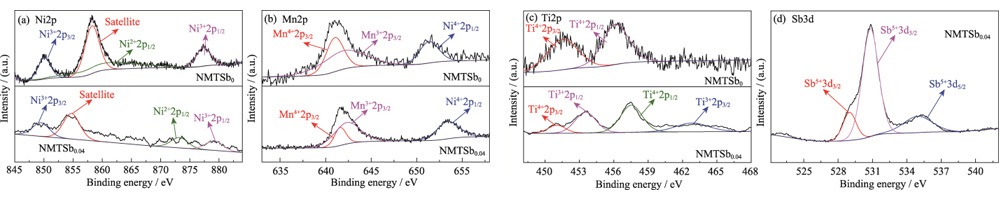
Fig. S2 (a) Espectros Ni2p, (b) Mn2p, (c) Ti2p e (d) Sb3d XPS de NMTSb0 e NMTSb0.04
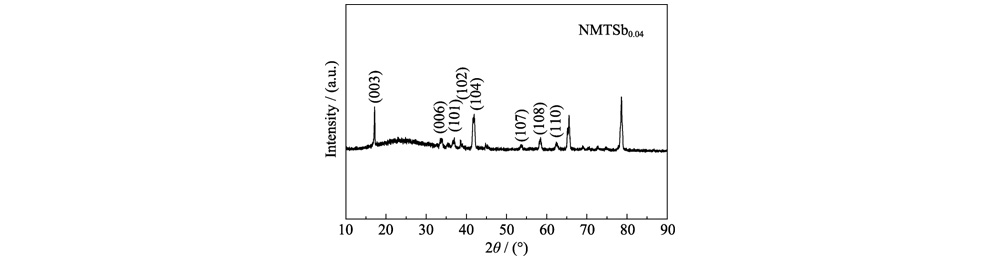
Fig. S3 DRX padrão de NMTSb0.04as material catódico de Bateria de íon Na após 200 ciclos
Tabela S1 resultados de ICP-AES de O3-NMTSbx (x=0, 0,02, 0,04, 0,06) (razão estequiométrica)
|
Na |
Ni |
Mn |
Ti |
Sb |
|
|
NMTSb0 |
0,913 |
0,486 |
0,288 |
0,181 |
0 |
|
NMTSb0.02 |
0,924 |
0,471 |
0,284 |
0,186 |
0,023 |
|
NMTSb0.04 |
0,920 |
0,452 |
0,287 |
0,184 |
0,039 |
|
NMTSb0,06 |
0,929 |
0,435 |
0,279 |
0,184 |
0,061 |
Tabela S2 Parâmetros de rede de materiais com NMTSb0 e NMTSb0,04
|
a/nm |
b/nm |
c/nm |
V/nm3 |
Rwp/% |
RP/% |
|
|
NMTSb0 |
0,29812 |
0,29812 |
1,600487 |
0,1232 |
4,92 |
5,53 |
|
NMTSb0.04 |
0,29790 |
0,29790 |
1,608391 |
0,1236 |
5,65 |
6,32 |



